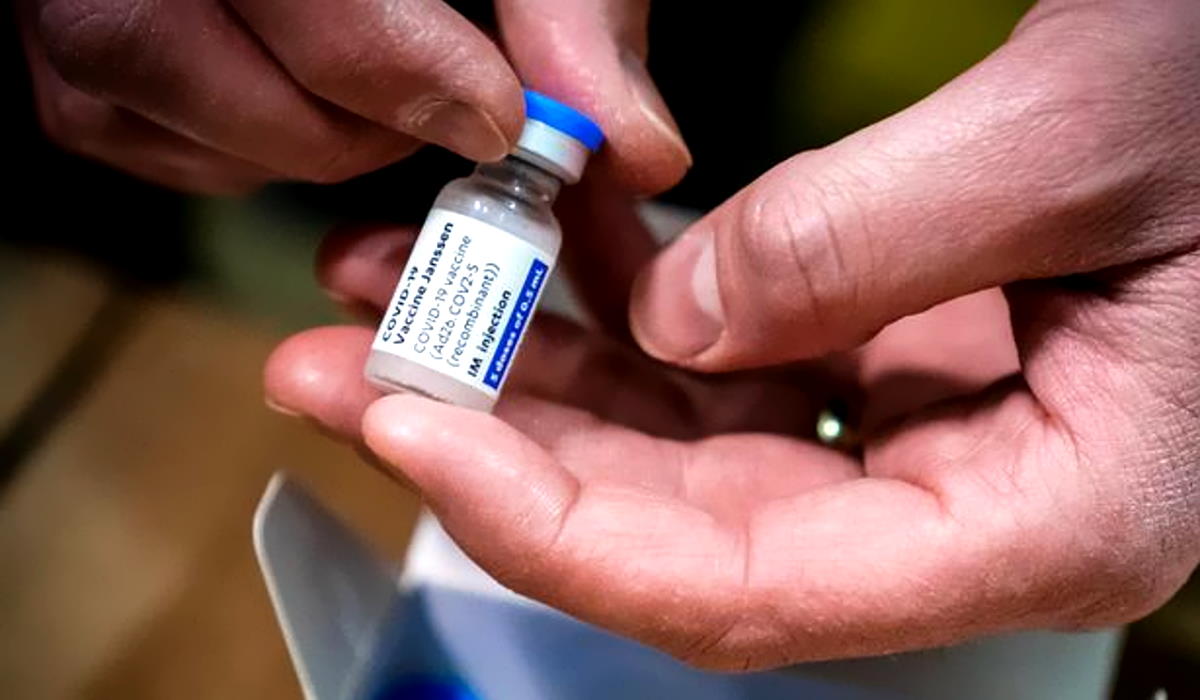
Trombosi del seno venoso cerebrale (CVST). Questa la diagnosi dei sei casi di trombosi che hanno interessato donne di età compresa tra i 18 e i 48 anni che si erano vaccinati contro il Covid utilizzando il prodotto di Johnson & Johnson (Janssen). I sintomi della trombosi si sono manifestati da 6 a 13 giorni dopo la vaccinazione.
A seguito di ciò, FDA e CDC, in una dichiarazione congiunta, hanno fatto sapere di averne temporaneamente sospeso la somministrazione. Attualmente, negli Stati Uniti ne sono state somministrate quasi 7 milioni di dosi. Quel vaccino è al momento l'unico che, in base al protocollo, non prevede un richiamo.
"Mercoledì - si legge nella nota - CDC convocherà una riunione del Comitato consultivo sulle pratiche di immunizzazione (ACIP) per esaminare ulteriormente questi casi. Altrettanto farà FDA. Finché il processo di valutazione non sarà completo, raccomandiamo una pausa nell'uso di questo vaccino per cautela. Ciò è importante, in parte, per garantire che la comunità degli operatori sanitari sia consapevole della possiblità di questi eventi avversi in modo da poterli riconoscere e gestire adeguatamente con il protocollo di cura previsto. causa del trattamento unico richiesto con questo tipo di coaguli di sangue".
Alla nota di FDA e CDC ha risposto, a sua volta con un comunicato, Johnson & Johnson dichiarando di condividerne il contenuto, di essere a conoscenza dei casi avversi, aggiungendo però che, al momento, non è stata stabilita una chiara relazione causale tra tali eventi, comunque rari, e il vaccino Janssen.
La notizia arriva nel momento in cui le prime dosi di Johnson & Johnson sono arrivate in Italia (184mila) e già molte regioni ne avevano programmato la somministrazione.
Proprio questo martedì, a seguito della procedura condotta a livello europeo su Vaxzevria, l'Agenzia Italiana del Farmaco ha comunicato agli operatori sanitari i seguenti elementi chiave relativi al vaccino prodotto da AstraZeneca:
- Una relazione causale tra la vaccinazione con Vaxzevria e l'insorgenza di trombosi in combinazione con trombocitopenia è considerata plausibile.
- Anche se tali reazioni avverse sono molto rare, hanno superato quanto atteso nella popolazione generale.
- In questa fase non sono stati identificati fattori di rischio specifici.
- Gli operatori sanitari devono vigilare su segni e sintomi di tromboembolia e/o trombocitopenia e informare di conseguenza i vaccinati.
- L'uso di questo vaccino deve essere conforme alle raccomandazioni ufficiali nazionali.
Nessuna comunicazione, finora, da parte di Aifa e di Ema sulla necessità o meno di fermare le vaccinazioni con il Johnson & Johnson in attesa di ulteriori verifiche e/o comunicazioni dagli Stati Uniti.
Aggiornamento
Nel pomeriggio i vertici dell'Aifa si sono riuniti con il ministro della Salute, Roberto Speranza. Così il ministro ne ha riassunto i contenuti durante la registrazione della puntata di martedì della trasmissione televisiva "Porta a Porta":
"C'è stata una scelta nelle ore immediatamente successive al pronunciamento dell'agenzia regolatoria statunitense da parte della stessa azienda: proprio Johnson&Johnson ha scelto infatti di rinviare per un tempo limitato l'immissione in commercio in tutti i paesi europei di questo vaccino. È un vaccino importante, aveva ed ha una caratteristica che per noi ha un particolare significato: riesce cioè ad immunizzare con una sola dose invece di due. È chiaro che rispetto alla scelta fatta dagli Stati Uniti, l'azienda ha scelto di non immettere sul mercato immediatamente il proprio vaccino in Europa e di fare prima i controlli sui dati americani. Oggi pomeriggio abbiamo fatto una riunione insieme ai nostri scienziati, con l'agenzia del farmaco italiana. Siamo in collegamento con l'agenzia europea e valuteremo nei prossimi giorni, appena Ema e gli americani ci daranno notizie più formali, quindi più definitive, quale sarà la strada migliore da intraprendere. Ma penso che anche questo vaccino dovrà essere utilizzato, perché è un vaccino importante.La scelta statunitense è una scelta precauzionale, così come quella di Johnson&Johnson di non immettere immediatamente in commercio in Europa il proprio siero. Il nostro auspicio è di poter presto sciogliere questi nodi e usare anche questo vaccino, che sarebbe il quarto e che a noi serve particolarmente".